Куда направляется лишнее железо?
Возможно, вы слышали о том, что помимо известных типов сахарного диабета (инсулинозависимый и инсулиннезависимый), существует еще один вариант — бронзовый диабет. Его не следует путать с бронзовой болезнью, известной как болезнь Аддисона, а также с пигментным циррозом или гемохроматозом.
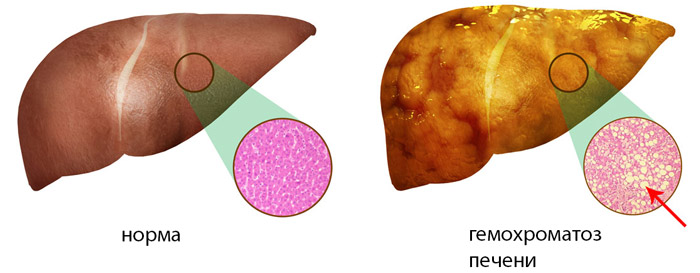
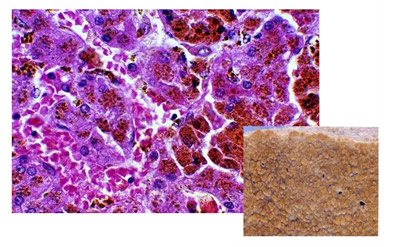
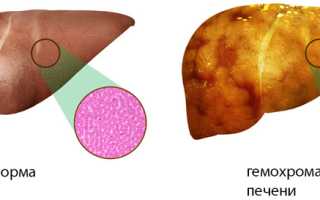
Первым под воздействием избытка железа оказывается печень (гемохроматоз печени). На начальных стадиях, когда другие органы еще не затронуты, портальные зоны печени начинают заполняться железом. Гемохроматоз печени приводит к замещению печеночной паренхимы соединительной тканью, что называется фиброзом. Это может развиться в цирроз, который в свою очередь вызывает серьезные последствия для этого жизненно важного органа.
Однако процесс не останавливается на печени. Железо продолжает накапливаться, достигая 20-60 граммов (при норме 4-5 г). Оно оседает в других паренхиматозных органах, что приводит к следующим последствиям:
- накопление в поджелудочной железе вызывает её дегенерацию;
- накопление в селезенке;
- накопление в миокарде создает условия для склероза коронарных сосудов;
- накопление в эпидермисе вызывает его истончение и атрофию;
- накопление в эндокринных железах (надпочечники, гипофиз, щитовидная железа, семенники).
Накопление железа в органах и тканях вызывает ответную реакцию, увеличивая скорость перекисного окисления липидов. Это приводит к повреждению клеточных органелл и развитию фиброза. Кроме того, происходит стимуляция продукции коллагена клетками, отвечающими за формирование соединительной ткани. Не имеет значения, в каких органах начинается накопление железа — если процесс не остановить, в конечном итоге пострадают все.
Токсичность железа заключается в том, что этот металл, обладая переменной валентностью (Fe (II), Fe (III)), легко инициирует свободнорадикальные реакции. Это повреждает клеточные органеллы и генетический материал клеток, усиливает продукцию коллагена и может провоцировать развитие опухолевых процессов.
Гемохроматоз представляет собой наследственное заболевание, связанное с избыточным накоплением железа в организме. Врачи отмечают, что заболевание развивается постепенно, проходя несколько стадий, начиная с бессимптомного накопления железа и заканчивая серьезными осложнениями, такими как цирроз печени или диабет. Основные формы гемохроматоза включают первичный, связанный с генетическими мутациями, и вторичный, возникающий на фоне других заболеваний.
Симптомы могут варьироваться от усталости и болей в суставах до более серьезных проявлений, таких как изменения кожи и нарушения функции печени. Диагностика включает анализы крови на уровень ферритина и трансферрина, а также генетические тесты. Лечение, как правило, заключается в регулярном кровопускании, что позволяет снизить уровень железа в организме. Врачи подчеркивают важность ранней диагностики и лечения, так как это значительно улучшает прогноз и качество жизни пациентов.

Как выглядит бронзовый диабет?
Накапливая важный металл, организм в течение года получает около 1 грамма железа, что может привести к избытку. При врожденном гемохроматозе запасы железа увеличиваются ежегодно и за 20 лет могут достичь значительных объемов — примерно 20 граммов (иногда до 50 г). Для сравнения: в норме в организме содержится около 4 граммов железа, распределенного между гемоглобином, миоглобином, дыхательными пигментами и ферментами. В запасе, в основном в печени, хранится до 0,5 г железа. Количество всасываемого элемента зависит от резервов организма: чем больше требуется железа, тем больше его должно поступать. При гемохроматозе повышенное всасывание приводит к избыточному накоплению.
Избыточное накопление железа происходит постепенно и проходит три стадии:
- Первая стадия — перегрузки железом нет (анализы в норме, клинические проявления отсутствуют).
- Вторая стадия — перегрузка уже наблюдается, что подтверждается лабораторными данными, но клинические симптомы пока не проявляются.
- Третья стадия — перегрузка железом приводит к характерной клинической симптоматике.
Таким образом, гемохроматоз становится заметным. Органы, накапливающие избыток железа, начинают страдать и теряют способность выполнять свои функции.
Симптомы гемохроматоза включают:
- Апатия, слабость и вялость.
- Увеличение и уплотнение печени (гепатомегалия), выброс ферритина, что может вызывать боли в животе и имитировать острые хирургические состояния. У пациентов с гемохроматозом печени риск развития первичного рака (гепатоцеллюлярной карциномы) составляет 30% среди тех, у кого уже диагностирован цирроз.
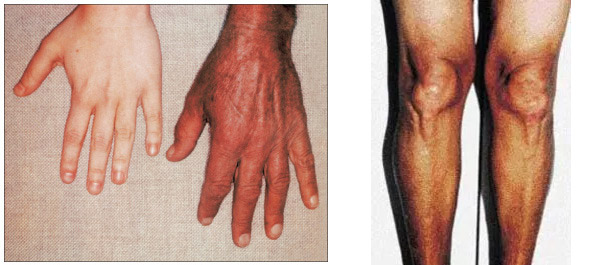
- Изменение цвета кожи (пигментация), затрагивающее подмышечные впадины, наружные половые органы и открытые участки тела.
- Сухость и истончение кожи.
- Снижение половой активности, импотенция, гинекомастия, атрофия яичек (у мужчин), бесплодие и аменорея (у женщин), выпадение волос на участках вторичного оволосения (из-за недостаточности гонадотропной функции гипофиза).
- Гемохроматоз сердца — поражение сердечной мышцы (до 90%), часто напоминающее кардиомиопатию, что приводит к прогрессирующей недостаточности правого предсердия и желудочка, аритмии и может закончиться инфарктом миокарда. Шаровидное сердце (форма) — «железное сердце» может внезапно остановиться, что приводит к смерти пациента.
- У 70-75% больных развивается сахарный диабет, вызванный повреждением паренхимы поджелудочной железы. Сахарный диабет при гемохроматозе приводит к осложнениям, характерным для других форм (нефропатия, поражения сетчатки глаз и периферических сосудов).
- Болезненные изменения в суставах (тазобедренных, коленных, плечевых, лучезапястных и других), вызванные отложением солей кальция. Характерный признак — тремор рук, сопровождаемый болевыми ощущениями.
Гемохроматоз может быть первичным или наследственным (врожденный гемохроматоз), возникающим из-за аутосомно-рецессивного нарушения обмена веществ и характеризующимся усиленным всасыванием железа в кишечнике. Вторичный или приобретенный гемохроматоз возникает из-за фоновой патологии, способствующей повышенному всасыванию железа в ЖКТ.
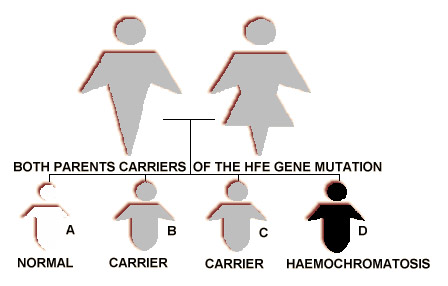
Человек наследует от обоих родителей ген с неблагоприятной информацией (аутосомно-рецессивный тип наследования). Однако пациент долгое время не подозревает о наличии проблемы, накапливая этот химический элемент ежедневно. Например, если в организме остается по 5 мг железа, поступающего с пищей, то первые симптомы могут проявиться примерно через 28 лет.
Гемохроматоз формируется на определенном этапе в результате различных нарушений. Не имеет значения, по какой причине произошло нарушение всасывания; важно, что железо накапливается в больших количествах в жизненно важных органах (сердце, печени, железах внутренней секреции, суставах), что мешает их нормальному функционированию.
| Характеристика | Подробности | Примечания |
|---|---|---|
| Развитие гемохроматоза | Наследственное нарушение метаболизма железа, приводящее к его избыточному накоплению в органах и тканях. Гены HFE (C282Y и H63D) наиболее часто мутируют. | Скорость накопления железа варьирует индивидуально. |
| Стадии гемохроматоза | 1. Латентная стадия (без симптомов, повышенное железо в сыворотке). 2. Ранняя стадия (повышенное железо в органах, минимальные симптомы). 3. Поздняя стадия (значительное накопление железа, выраженные симптомы поражения органов). | Диагностика на ранних стадиях критически важна для предотвращения осложнений. |
| Формы гемохроматоза | Наследственный гемохроматоз (тип 1 – наиболее распространенный, связан с мутациями гена HFE; тип 2 – редкие формы с мутациями других генов; тип 3 – ювенильный гемохроматоз); Вторичный гемохроматоз (связан с другими заболеваниями, например, талассемией, анемией). | Лечение зависит от типа гемохроматоза. |
| Симптомы гемохроматоза | Усталость, слабость, боль в суставах, артрит, бронзовый загар кожи, увеличение печени и селезенки, диабет, сердечная недостаточность, цирроз печени, импотенция, снижение либидо. | Симптомы могут быть неспецифическими и проявляться постепенно. |
| Диагностика гемохроматоза | Определение уровня ферритина в сыворотке крови, трансферрина, насыщения трансферрина железом, генетическое тестирование (на мутации генов HFE), биопсия печени (оценка содержания железа в печени). | Комплексный подход к диагностике необходим для подтверждения диагноза и исключения других заболеваний. |
| Лечение гемохроматоза | Флеботомия (регулярное кровопускание) – основной метод лечения; хелатирующие агенты (дефероксамин, деферасирокс) – для выведения железа из организма; диета с ограничением железа. | Лечение должно быть пожизненным и контролироваться врачом. |
| Прогноз гемохроматоза | При своевременной диагностике и лечении прогноз благоприятный. Без лечения возможно развитие серьезных осложнений, таких как цирроз печени, сердечная недостаточность, диабет, рак печени. | Регулярный мониторинг состояния здоровья и соблюдение рекомендаций врача крайне важны. |
Наследственный или первичный гемохроматоз
Наследственный гемохроматоз
Наследственный гемохроматоз (НГ) оказывается довольно распространенной болезнью, хотя ранее считалось иначе из-за отсутствия массовых популяционно-генетических исследований.
В 70-х годах прошлого века, когда активно изучался главный комплекс гистосовместимости (МНС), подтвердилось предположение о генетической природе первичного гемохроматоза. В это время открывались антигены лейкоцитарной системы HLA, и стало известно, что ген, отвечающий за уровень железа в организме, находится на коротком плече 6-й хромосомы, рядом с локусом А (А3) комплекса HLA. Это привело к выявлению связи между гемохроматозом и генами главной системы гистосовместимости.
Первичный гемохроматоз всегда наследственный. Он появляется в популяции с рождением нового (гомозиготного) индивида, но проявляется лишь через 2-3 десятилетия.
Современные исследования показывают, что распространенность дефектного рецессивного гена гемохроматоза, нарушающего обмен веществ и приводящего к повышенному всасыванию железа, составляет до 10% среди населения. Гомозиготные носители рецессивного гена встречаются с частотой 0,3-0,45%. Это означает, что в Европе примерно один из трехсот человек может родиться с такими отклонениями. При этом 10% европейцев, являясь носителями гена гемохроматоза (гетерозиготы), не могут быть уверены, что эта патология не затронет их или их детей. Клинические формы гемохроматоза печени, связанные с врожденным дефектом гена, возникают с частотой 2 случая на 1000 человек.
Гетерозиготы также не должны расслабляться. Хотя вероятность развития избытка железа у них невелика (не превышает 4%), наличие гена гемохроматоза может быть не таким безобидным, как кажется. У носителей могут наблюдаться признаки ускоренного всасывания и повышенного содержания железа в организме, особенно если они страдают от других заболеваний, влияющих на обмен железа, таких как гепатит С или злоупотребление алкоголем.
Ранее наследственный гемохроматоз рассматривался как простая моногенная патология, но в настоящее время его классифицируют в зависимости от генетических дефектов и симптомов. Выделяют четыре типа первичного гемохроматоза:
- I тип – самый распространенный (до 95%) аутосомно-рецессивный (классический), ассоциированный с HFE, вызванный мутацией гена HFE (точечная мутация – С282У);
- II тип – ювенильный;
- III тип – HFE-неассоциированный (мутация в трансферриновом рецепторе 2 типа);
- IV тип – аутосомно-доминантный гемохроматоз.
Основой развития первичного врожденного гемохроматоза являются мутации гена HFE, которые нарушают захват железа энтероцитами (клетками 12-перстной кишки) с участием трансферрина. В результате поступает искаженная информация о снижении уровня железа в организме, и энтероциты начинают активно производить связывающий железо белок – DCT-1, что приводит к усиленному захвату железа и его накоплению в избытке внутри клеток.
Гемохроматоз — это наследственное заболевание, связанное с избыточным накоплением железа в организме. Люди, страдающие от этой патологии, часто отмечают, что симптомы могут проявляться постепенно: усталость, боли в суставах, изменения в коже. На ранних стадиях заболевание может быть бессимптомным, что затрудняет диагностику. Важно проводить регулярные анализы на уровень ферритина и трансферрина, чтобы выявить проблему на раннем этапе. Лечение обычно включает флеботомию — регулярное удаление крови для снижения уровня железа. Прогноз при своевременной диагностике и лечении может быть благоприятным, однако запущенные формы могут привести к серьезным осложнениям, включая заболевания печени и сердца. Поэтому важно быть внимательным к своему здоровью и обращаться к врачу при первых признаках.

Приобретенный вариант
Вторичный гемохроматоз, или генерализованный гемосидероз, — это приобретённая форма гемохроматоза, развивающаяся на фоне уже существующих заболеваний. К ним относятся неэффективный эритропоэз (например, мегалобластная анемия или рефрактерная анемия при миелодиспластическом синдроме), гемолитическая анемия, хронические заболевания печени, а также чрезмерное употребление препаратов с железом и избыточное потребление железа с пищей. В этих случаях причиной вторичного гемохроматоза становится истощение ферментных систем, участвующих в обмене железа.
Также вторичный гемохроматоз может возникать из-за парентеральной перегрузки железом, связанной с трансфузиями эритроцитарной массы и введением железа с декстраном (посттрансфузионный гемохроматоз). Например, пациенты с апластической анемией, получающие большое количество донорских эритроцитов, могут испытывать перегрузку железом. Важно, чтобы врачи учитывали необходимость профилактики вторичного гемохроматоза у таких пациентов, особенно если они не теряют кровь, и назначали препараты, связывающие избыточное железо и образующие с ним хелатные соединения.
Помимо посттрансфузионного гемохроматоза, выделяют и другие формы этой вторичной патологии:
- Алиментарный гемохроматоз — развивается после цирроза печени, вызванного чрезмерным употреблением алкоголя;
- Метаболический гемохроматоз — возникает из-за нарушений обменных процессов, связанных с железом (например, промежуточная талассемия, некоторые вирусные гепатиты, злокачественные опухоли);
- Смешанный гемохроматоз — наблюдается при бета-талассемии и анемических синдромах, возникающих на фоне нарушений эритропоэза;
- Неонатальный гемохроматоз — проявляется у новорожденных с перегрузкой железом. Эта патология может проявляться в первые дни жизни, сопровождается задержкой внутриутробного развития и печеночной недостаточностью, и, к сожалению, может привести к летальному исходу в течение нескольких дней.
Что же происходит, когда начинается активное всасывание Fe
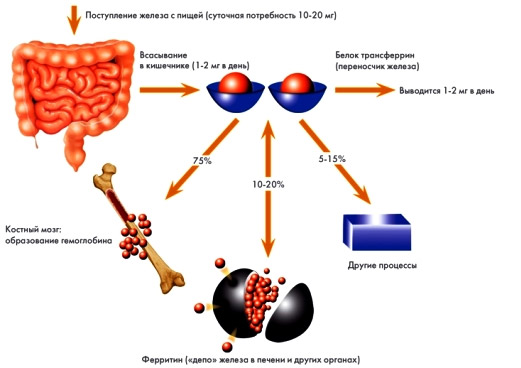
Европейцы в среднем потребляют около 10-20 мг железа (Fe) с пищей в виде различных соединений. В сутки через желудочно-кишечный тракт в организм поступает 1-2 мг этого элемента, и такое же количество выводится. У людей с нехваткой железа, наследственным гемохроматозом или заболеваниями, связанными с нарушением образования эритроцитов, уровень всасываемого железа может увеличиваться примерно в три раза. Процесс абсорбции активен и происходит в тонком кишечнике (в его верхней части):
- Железо попадает в клетки кишечной слизистой и накапливается в их жидком содержимом.
- Часть железа сохраняется в форме ферритина (гидроокись Fe (III) + белок апоферритин) для дальнейшего использования в синтезе гемоглобина и других железосодержащих соединений. Основная задача ферритина — транспортировка всосавшегося железа к трансферрину, который переносит Fe по кровеносной системе.
- Трансферрин захватывает железо, насыщается им примерно на одну треть (это та доля, которая участвует в обменных процессах) и доставляет его к месту назначения.
- Комплекс «трансферрин + Fe» проникает в клетку, где железо освобождается от транспортного белка. Когда в клетке накапливается достаточное количество железа, активность рецепторов трансферрина снижается.
Эти процессы происходят корректно только при нормальном обмене железа в организме. При гемохроматозе наблюдается избыточное накопление железа, которое не может сохраняться в форме ферритина. Молекулы железосодержащего белка начинают распадаться, образуя гемосидерин, уровень которого при гемохроматозе значительно повышается. Это состояние часто называют гемосидерозом.
При избытке железа транспортному белку приходится работать в условиях перегрузки, и он вынужден забирать не одну треть, а значительно больше, достигая полного насыщения. Однако это не решает проблему, так как железо продолжает накапливаться и начинает перемещаться самостоятельно (без трансферрина) в виде различных соединений с низкомолекулярными хелаторами, которые действуют как ловушки для Fe. Эта форма позволяет железу легко проникать в клетки, независимо от его необходимости. Перенасыщенная железом клетка не может препятствовать поступлению новой порции металла, который становится избыточным.

Диагностика
Диагностика гемохроматоза не зависит от источника заболевания и остается одинаковой для всех его форм.
Подозрение на избыточное накопление железа может возникнуть на основании жалоб и клинических проявлений. У мужчин наличие наследственного гемохроматоза можно предположить по симптомам, таким как увеличение печени, общая слабость, боли в суставах и изменения в активности трансфераз (АлТ, АсТ). Однако стоит отметить, что их показатели редко имеют значительные отклонения от нормы, даже при явных признаках цирроза печени. На первом этапе диагностики врач направляет пациента на ультразвуковое исследование (УЗИ) и магнитно-резонансную томографию (МРТ), а также назначает ряд лабораторных анализов:
- Генетическое тестирование для выявления точечных мутаций, характерных для наследственного гемохроматоза (С282У и H63D) в гене гемохроматоза;
- Определение уровня сывороточного железа;
- Общая железосвязывающая способность сыворотки (ОЖСС) или процент насыщения трансферрина железом – этот анализ показывает, сколько транспортного белка, связанного с переносом железа, содержится в сыворотке крови (в норме – около 30%);
- Уровень ферритина в сыворотке крови для оценки запасов железа в организме.
Если все проведенные исследования подтверждают наличие гемохроматоза, целесообразно провести биопсию печени для окончательной установки диагноза. На начальном этапе у молодых пациентов избыточные запасы железа будут заметны только в клетках печени (гепатоцитах) и в перипортальной области. У пожилых людей отложения могут наблюдаться как в гепатоцитах, так и в клетках Купфера и желчных протоках. Цирроз печени при гемохроматозе обычно имеет мелкоузловую (микронодулярную) форму.
При выявлении изменений в печени и наличии разрастания соединительной ткани (цирроза) необходимо провести дифференциальную диагностику. В этом поможет гистологическое исследование (биопсия), так как замещение печеночной ткани соединительной при гепатитах или злоупотреблении алкоголем имеет свои особенности.
Гепатоцеллюлярную карциному на фоне гемохроматоза можно заподозрить, если состояние пациента за последнее время значительно ухудшилось, наблюдается выраженное увеличение печени и повышение уровня опухолевого маркера – α-фетопротеина.
Лечение, профилактика, прогноз
Лечение начинается с пересмотра питания. Все продукты, содержащие железо, должны быть исключены из рациона. Основным медикаментозным средством является препарат, который образует комплекс с железом и способствует его выведению из организма. Кровопускания также положительно влияют при гемохроматозе: они уменьшают размеры печени и селезенки, снижают пигментацию, улучшают показатели печеночных ферментов и в некоторых случаях облегчают лечение сахарного диабета. Часто одновременно применяются экстракорпоральные методы, такие как гемосорбция и плазмаферез, которые помогают удалить избыток железа.
При лечении гемохроматоза не забывают и о симптоматической терапии, так как у многих пациентов уже могут наблюдаться изменения в печени, сердце и других органах. В некоторых случаях симптоматическое лечение становится серьезным, например, может потребоваться пересадка печени при циррозе или эндопротезирование поврежденных суставов (артропластика).
Профилактика гемохроматоза заключается в раннем выявлении заболевания. Это включает определение уровня железа, ферритина и трансферрина, а также проведение генетического анализа (обследование близких родственников пациента), что особенно важно при бессимптомном течении у молодых людей.
Прогноз при гемохроматозе в целом благоприятный, если процесс не затронул печеночную паренхиму и не привел к циррозу. В таком случае гемохроматоз не сказывается на продолжительности жизни. В остальных случаях все зависит от степени поражения печени и длительности перегрузки железом. Чаще всего пациенты с гемохроматозом умирают от диабетической или печеночной комы, сердечной недостаточности или желудочно-кишечных кровотечений, вызванных варикозным расширением вен, а также от первичного рака печени. Однако ранняя диагностика и своевременное лечение гемохроматоза могут предотвратить серьезные последствия.
Видео: лекция по гемохроматозу
Перейти в раздел:
- Заболевания крови, её состав, анализы и биохимические исследования
Советы от СосудИнфо предоставляют квалифицированные специалисты с высшим медицинским образованием и практическим опытом.
Вопрос-ответ
Как лечится гемохроматоз?
Лечение направлено на снижение уровня железа в организме с помощью регулярных процедур введения венозных средств для удаления избытка железа, диеты с ограничением потребления железа. Другие названия заболевания: пигментный цирроз, бронзовый диабет.
Как долго живут люди с гемохроматозом?
При отсутствии лечения болезнь гемохроматоз способна унести жизнь человека в течение 5 лет в результате развития тяжелых осложнений.
Какой уровень железа в крови может указывать на гемохроматоз?
На заболевание может указывать уровень железа в крови выше 27 мкмоль/л, насыщение трансферрина железом более 45%, концентрация ферритина в плазме 350–500 нг/мл. Чтобы оценить работу внутренних органов и выявить нарушения со стороны печени и почек, может быть рекомендовано биохимическое исследование крови.
Чем опасен гемохроматоз?
Избыток железа может накапливаться в органах, приводя к нарушению их работы и возникновению заболеваний. Особенно этому подвержены печень, сердце и поджелудочная железа. Слишком много железа может привести к опасным для жизни состояниям, таким как цирроз печени, сердечная недостаточность и сахарный диабет.
Советы
СОВЕТ №1
Регулярно проходите медицинские обследования, особенно если у вас есть семейная история гемохроматоза. Раннее выявление заболевания может значительно улучшить прогноз и снизить риск осложнений.
СОВЕТ №2
Обратите внимание на свою диету. Ограничьте потребление продуктов, богатых железом, таких как красное мясо и печень, а также избегайте добавок с железом, если это не предписано врачом.
СОВЕТ №3
Следите за симптомами и не игнорируйте их. Если вы заметили усталость, боли в суставах или изменения в цвете кожи, обязательно проконсультируйтесь с врачом для дальнейшей диагностики.
СОВЕТ №4
Обсудите с врачом возможность регулярного кровопускания или других методов лечения, которые могут помочь снизить уровень железа в организме. Это может быть важной частью управления заболеванием.